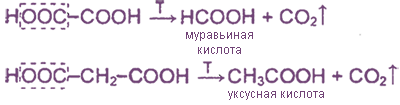Карбоновые кислоты
Общая формула
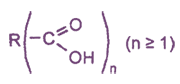
Классификация
СН3СН2СН2СООН;
НООС-СН2-СООН пропандиовая (малоновая) кислота

предельные; например: СН3СН2СООН;
непредельные; например: СН2=СНСООН пропеновая(акриловая) кислота
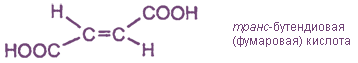


Предельные монокарбоновые кислоты
(одноосновные насыщенные карбоновые кислоты) – карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой -COOH. Все они имеют общую формулу
Номенклатура
Систематические названия одноосновных предельных карбоновых кислот даются по названию соответствующего
1. НСООН метановая (муравьиная) кислота
2. СН3СООН этановая (уксусная) кислота
3. СН3СН2СООН пропановая (пропионовая) кислота
Изомерия
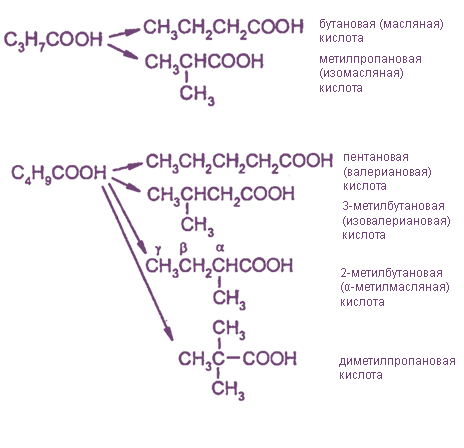
Изомерия скелета в углеводородном радикале проявляется, начиная с бутановой кислоты, которая имеет два изомера:
Межклассовая изомерия проявляется, начиная с уксусной кислоты:
- CH3-COOH уксусная кислота;
- H-COO-CH3 метилформиат (метиловый эфир муравьиной кислоты);
- HO-CH2-COH гидроксиэтаналь (гидроксиуксусный альдегид);
- HO-CHO-CH2 гидроксиэтиленоксид.
Гомологический ряд
Тривиальное название |
Название по ИЮПАК |
Формула |
Муравьиная кислота |
Метановая кислота |
HCOOH |
Уксусная кислота |
Этановая кислота |
CH3COOH |
Пропионовая кислота |
Пропановая кислота |
C2H5COOH |
Масляная кислота |
Бутановая кислота |
C3H7COOH |
Валериановая кислота |
Пентановая кислота |
C4H9COOH |
Капроновая кислота |
Гексановая кислота |
C5H11COOH |
Энантовая кислота |
Гептановая кислота |
C6H13COOH |
Каприловая кислота |
Октановая кислота |
C7H15COOH |
Пеларгоновая кислота |
Нонановая кислота |
C8H17COOH |
Каприновая кислота |
Декановая кислота |
C9H19COOH |
Ундециловая кислота |
Ундекановая кислота |
C10H21COOH |
... |
... |
... |
Пальмитиновая кислота |
Гексадекановая кислота |
C15H31COOH |
Стеариновая кислота |
Октадекановая кислота |
C17H35COOH |
Кислотные остатки и кислотные радикалы
Кислота |
Кислотный остаток |
Кислотный радикал (ацил) |
НСООН |
НСОО- |
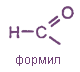 |
СН3СООН |
СН3СОО- |
|
СН3СН2СООН |
СН3СН2СОО- |
|
СН3(СН2)2СООН |
СН3(СН2)2СОО- |
|
СН3(СН2)3СООН |
СН3(СН2)3СОО- |
|
СН3(СН2)4СООН |
СН3(СН2)4СОО- |
Электронное строение молекул карбоновых кислот
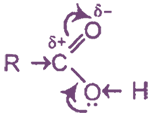
Показанное в формуле смещение электронной плотности в сторону карбонильного атома кислорода обусловливает сильную поляризацию связи О-Н, в результате чего облегчается отрыв атома водорода в виде протона - в водных растворах происходит процесс кислотной диссоциации:
RCOOH ↔ RCOO- + Н+
В карбоксилат-ионе (RCOO-) имеет место р, π-сопряжение неподеленной пары электронов атома кислорода гидроксильной группы с р-облаками, образующими π- связь, в результате происходит делокализация π- связи и равномерное распределение отрицательного заряда между двумя атомами кислорода:
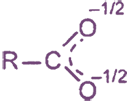
В связи с этим для карбоновых кислот, в отличие от альдегидов, не характерны реакции присоединения.
Физические свойства

Температуры кипения кислот значительно выше температур кипения спиртов и альдегидов с тем же числом атомов углерода, что объясняется образованием циклических и линейных ассоциатов между молекулами кислот за счет водородных связей:
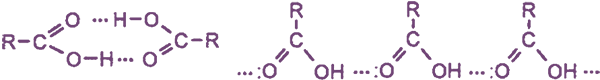
Химические свойства
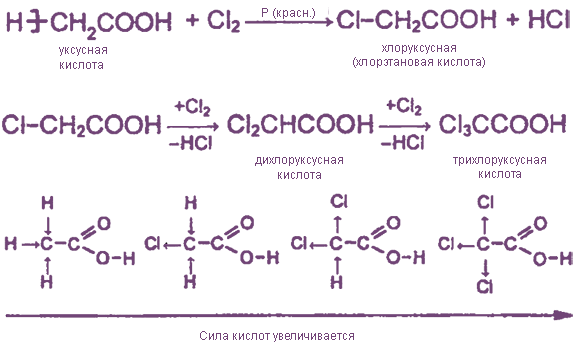
I. Кислотные свойства
Сила кислот уменьшается в ряду:
НСООН → СН3СООН → C2H6COOH → ...
1. Реакции нейтрализации
СН3СООН + КОН → СН3СООК + н2O
2. Реакции с основными оксидами
2HCOOH + СаО → (НСОО)2Са + Н2O
3. Реакции с металлами
2СН3СН2СООН + 2Na → 2СН3СН2COONa + H2↑
4. Реакции с солями более слабых кислот (в т. ч. с карбонатами и гидрокарбонатами)
2СН3СООН + Na2CO3 → 2CH3COONa + CO2↑ + Н2O
2НСООН + Mg(HCO3)2 → (НСОО)2Мg + 2СO2↑ + 2Н2O
(НСООН + НСО3- → НСОО- + СO2 +Н2O)
5. Реакции с аммиаком
СН3СООН + NH3 → CH3COONH4
II. Замещение группы -ОН
1. Взаимодействие со спиртами (реакции этерификации)
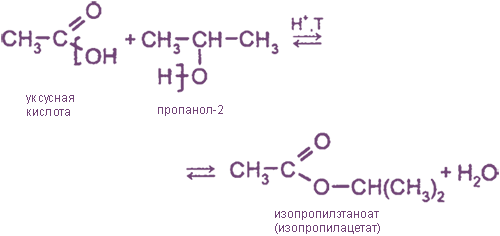
2. Взаимодействие с NH3 при нагревании (образуются амиды кислот)
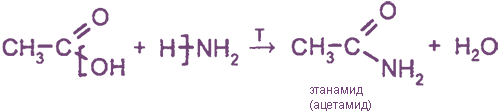
Амиды кислот 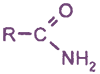 гидролизуются с образованием кислот:
гидролизуются с образованием кислот:
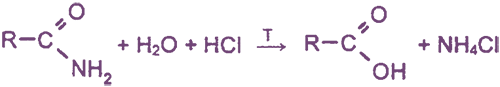
или их солей:

3. Образование галогенангидридов
Наибольшее значение имеют
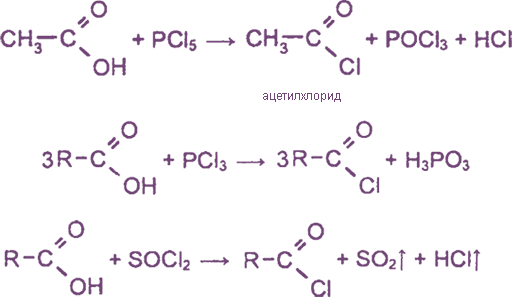
4. Образование ангидридов кислот (межмолекулярная дегидратация)

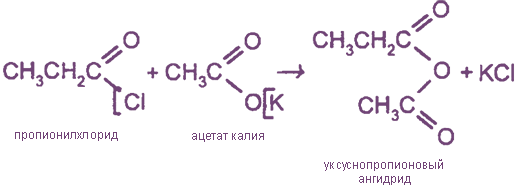
Ангидриды кислот образуются также при взаимодействии хлорангидридов кислот с безводными солями карбоновых кислот; при этом можно получать смешанные ангидриды различных кислот; например:
Особенности строения и свойств муравьиной кислоты
Строение молекулы
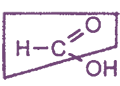
Молекула муравьиной кислоты, в отличие от других карбоновых кислот, содержит в своей структуре
Химические свойства
Муравьиная кислота вступает в реакции, характерные как для кислот, так и для альдегидов. Проявляя свойства альдегида, она легко окисляется до угольной кислоты:

В частности, НСООН окисляется аммиачным раствором Ag2O и гидроксидом меди (II) Сu(ОН)2, т. е. дает качественные реакции на альдегидную группу:
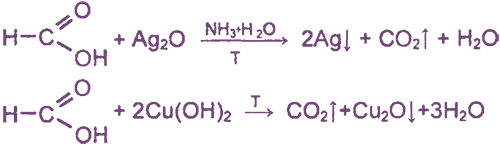
При нагревании с концентрированной H2SO4 муравьиная кислота разлагается на оксид углерода (II) и воду:

Муравьиная кислота заметно сильнее других алифатических кислот, так как карбоксильная группа в ней связана с атомом водорода, а не с электроно-донорным алкильным радикалом.
Способы получения предельных монокарбоновых кислот
1. Окисление спиртов и альдегидов
Общая схема окисления спиртов и альдегидов:
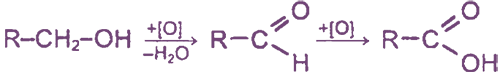
В качестве окислителей используют KMnO4, K2Cr2O7, HNO3 и другие реагенты.
Например:
5С2Н5ОН + 4KMnO4 + 6H2S04 → 5СН3СООН + 2K2SO4 + 4MnSO4 + 11Н2O
2. Гидролиз сложных эфиров
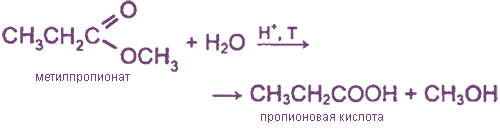
3. Окислительное расщепление двойных и тройных связей в алкенах и в алкинах
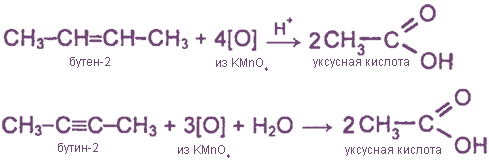
Способы получения НСООН (специфические)
1. Взаимодействие оксида углерода (II) с гидроксидом натрия
СO + NaOH → HCOONa формиат натрия
2HCOONa + H2SO4 → 2НСООН + Na2SO4
2. Декарбоксилирование щавелевой кислоты
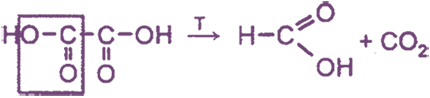
Способы получения СН3СООН (специфические)
1. Каталитическое окисление бутана
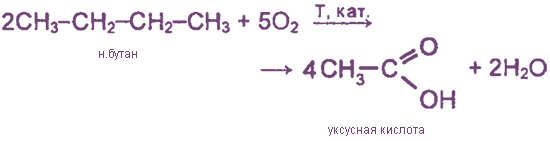
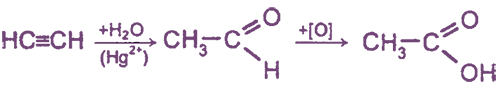
2. Синтез из ацетилена
3. Каталитическое карбонилирование метанола

4. Уксуснокислое брожение этанола
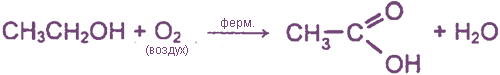
Так получают пищевую уксусную кислоту.
Получение высших карбоновых кислот
Гидролиз природных жиров
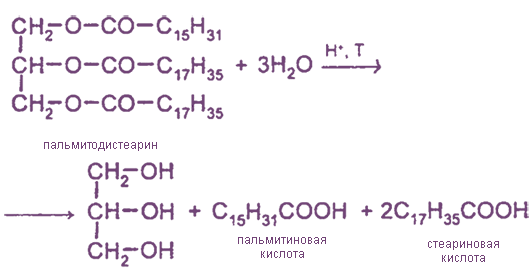
Непредельные монокарбоновые кислоты
Важнейшие представители
Общая формула алкеновых кислот:
CH2=CH-COOH пропеновая (акриловая) кислота
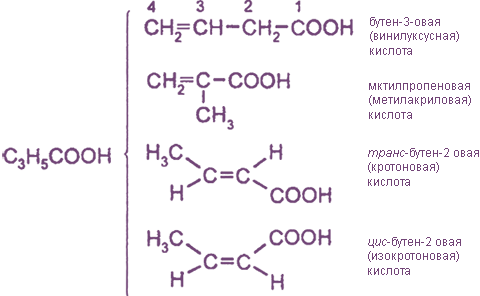
Высшие непредельные кислоты
Радикалы этих кислот входят в состав растительных масел.
C17H33COOH - олеиновая кислота, или цис-октадиен-9-овая кислота
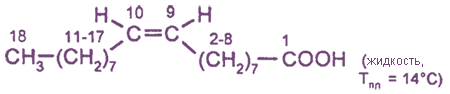
Транс-изомер олеиновой кислоты называется элаидиновой кислотой.
C17H31COOH - линолевая кислота, или цис, цис-октадиен-9,12-овая кислота
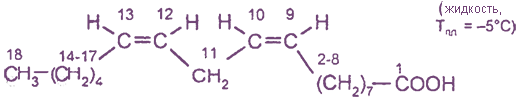
C17H29COOH - линоленовая кислота, или цис, цис, цис-октадекатриен-9,12,15-овая кислота
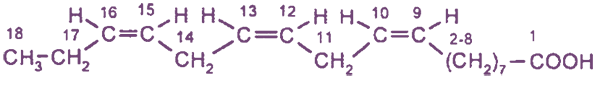
Особенности химических свойств
Кроме общих свойств карбоновых кислот, для непредельных кислот характерны реакции присоединения по кратным связям в углеводородном радикале. Так, непредельные кислоты, как и алкены, гидрируются и обесцвечивают бромную воду, например:
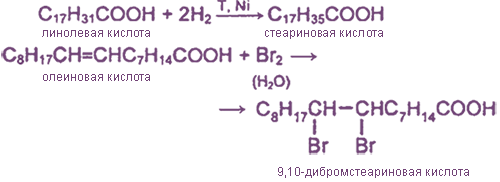
Отдельные представители дикарбоновых кислот
Предельные дикарбоновые кислоты HOOC-R-COOH

HOOC-CH2-COOH пропандиовая (малоновая) кислота, (соли и эфиры - малонаты)
HOOC-(CH2)2-COOH бутадиовая (янтарная) кислота, (соли и эфиры - сукцинаты)
HOOC-(CH2)3-COOH пентадиовая (глутаровая) кислота, (соли и эфиры - глутораты)
HOOC-(CH2)4-COOH гексадиовая (адипиновая) кислота, (соли и эфиры - адипинаты)
Особенности химических свойств
Дикарбоновые кислоты во многом сходны с монокарбоновыми, однако являются более сильными. Например, щавелевая кислотасильнее уксусной почти в 200 раз.
Дикарбоновые кислоты ведут себя как двухосновные и образуют два ряда солей - кислые и средние:
HOOC-COOH + NaOH → HOOC-COONa + H2O
HOOC-COOH + 2NaOH → NaOOC-COONa + 2H2O
При нагревании щавелевая и малоновая кислоты легко декарбоксилируются: