Непредельные углеводороды. Алкены
Простейшим алкеном является этен C2H4.По номенклатуре IUPAC названия алкенов образуются от названий соответствующих алканов заменой суффикса
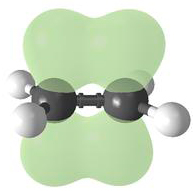
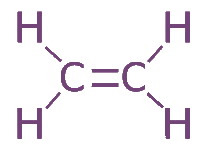

Пространственная структура этилена
По названию первого представителя этого ряда - этилена - такие углеводороды называют
Номенклатура и изомерия
Номенклатура
Алкены простого строения часто называют, заменяя суффикс
По систематической номенклатуре названия этиленовых углеводородов производят заменой суффикса -ан в соответствующих алканах на суффикс -ен (алкан - алкен, этан - этен, пропан - пропен и т.д.). Выбор главной цепи и порядок названия тот же, что и для алканов. Однако в состав цепи должна обязательно входить двойная связь. Нумерацию цепи начинают с того конца, к которому ближе расположена эта связь. Например:
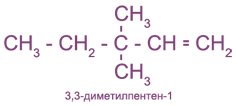
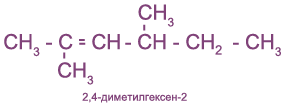
Иногда используют и рациональные названия. В этом случае все алкеновые углеводороды рассматривают как замещенные этилена:
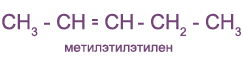
Непредельные (алкеновые) радикалы называют тривиальными названиями или по систематической номенклатуре:
Изомерия
Для алкенов характерны два вида структурной изомерии. Кроме изомерии, связанной со строением углеродного скелета (как у алканов), появляется изомерия, зависящая от положения двойной связи в цепи. Это приводит к увеличению числа изомеров в ряду алкенов.
Первые два члена гомологического ряда алкенов -(этилен и пропилен) - изомеров не имеют и их строение можно выразить так:
H2C = CH2 этилен (этен)
H2C = CH - CH3 пропилен (пропен)
Изомерия положения кратной связи
H2C = CH - CH2 - CH3 бутен-1
H3C - CH = CH - CH3 бутен-2
Геометрическая изомерия - цис-, транс- изомерия.
Такая изомерия характерна для соединений с двойной связью.
Если простая σ -связь допускает свободное вращение отдельных звеньев углеродной цепи вокруг своей оси, то вокруг двойной связи такого вращения не происходит. Это и является причиной появления геометрических (цис-, транс-) изомеров.
Геометрическая изомерия - один из видов пространственной изомерии.
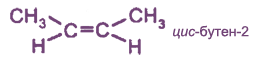
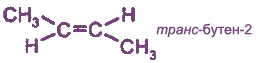
Цис- и транс-изомеры отличаются не только пространственным строением, но и многими физическими и химическими свойствами. Транс-изомеры более устойчивы, чем цис-изомеры.
Получение алкенов
В природе алкены встречаются редко. Обычно газообразные алкены (этилен, пропилен, бутилены) выделяют из газов нефтепереработки (при крекинге) или попутных газов, а также из газов коксования угля.
Дегидрирование алканов
H3C - CH2 - CH2 - CH3 → H2C = CH - CH2 - CH3 + H2↑ (бутен-1)
бутан
H3C - CH2 - CH2 - CH3 → H3C - CH = CH - CH3 + H2↑ (бутен-2)
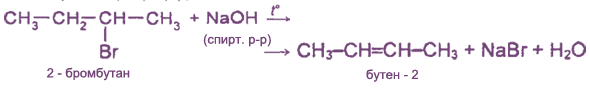
H-C ≡ C-H + H2 → H2C = CH2
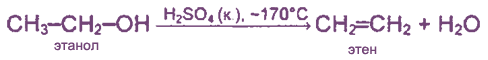
В таких реакциях
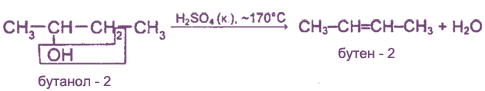
Физические свойства
Физические свойства некоторых алкенов показаны в таблице ниже. Первые три представителя гомологического ряда алкенов (этилен, пропилен и бутилен) - газы, начиная с C5H10 (амилен, или пентен-1) - жидкости, а с С18Н36 - твердые вещества. С увеличением молекулярной массы повышаются температуры плавления и кипения. Алкены нормального строения кипят при более высокой температуре, чем их изомеры, имеющие изостроение. Температуры кипения цис-изомеров выше, чем транс-изомеров, а температуры плавления - наоборот.
Алкены плохо растворимы в воде (однако лучше, чем соответствующие алканы), но хорошо - в органических растворителях. Этилен и пропилен горят коптящим пламенем.
Физические свойства некоторых алкенов
Название |
Формула |
t пл,°С |
t кип,°С |
d204 |
Этилен (этен) |
С2Н4 |
-169,1 |
-103,7 |
0,5700 |
Пропилен (пропен) |
С3Н6 |
-187,6 |
-47,7 |
0,5193* |
Бутилен (бутен-1) |
C4H8 |
-185,3 |
-6,3 |
0,5951 |
Цис-бутен-2 |
С4Н8 |
-138,9 |
3,7 |
0,6213 |
Транс-бутен-2 |
С4Н8 |
-105,5 |
0,9 |
0,6042 |
Изобутилен (2-метилпропен) |
С4Н8 |
-140,4 |
-7,0 |
0,5942* |
Амилен (пентен-1) |
C5H10 |
-165,2 |
+30,1 |
0,6405 |
Гексилен (гексен-1) |
С6Н12 |
-139,8 |
63,5 |
0,6730 |
Гептилен (гептен-1) |
C7H14 |
-119 |
93,6 |
0,6970 |
Октилен (октен-1) |
C8H16 |
-101,7 |
121,3 |
0,7140 |
Нонилен (нонен-1) |
C9H18 |
-81,4 |
146,8 |
0,7290 |
Децилен (децен-1) |
С10Н20 |
-66,3 |
170,6 |
0,7410 |
* Жидкий
Алкены малополярны, но легко поляризуются.
Химические свойства
Алкены обладают значительной реакционной способностью. Их химические свойства определяются, главным образом, двойной углерод-углеродной связью.
π-Связь, как наименее прочная и более доступная, при действии реагента разрывается, а освободившиеся валентности углеродных атомов затрачиваются на присоединение атомов, из которых состоит молекула реагента. Это можно представить в виде схемы:
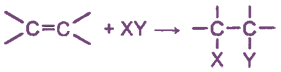
Таким образом, при реакциях присоединения двойная связь разрывается как бы наполовину (с сохранением σ-связи).
Реакции присоединения
Чаще реакции присоединения идут по гетеролитическому типу, являясь реакциями электрофильного присоединения.
Н2С = СН2 + H2 → Н3С - СН3 (этан)
этилен
Н2С = СН2 + Cl2 → ClH2C - CH2Cl (1,2-дихлорэтан)
Легче идет присоединение хлора и брома, труднее — иода. Фтор с алкенами, как и с алканами, взаимодействует со взрывом.
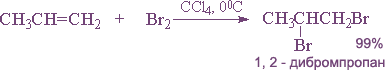
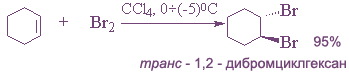
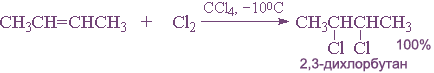
Реакцию галогенирования обычно проводят в растворителе при обычной температуре.
Присоединение брома и хлора к алкенам происходит по ионному, а не по радикальному механизму. Этот вывод следует из того, что скорость присоединения галогена не зависит от облучения, присутствия кислорода и других реагентов, инициирующих или ингибирующих радикальные процессы. На основании большого числа экспериментальных данных для этой реакции был предложен механизм, включающий несколько последовательных стадий. На первой стадии происходит поляризация молекулы галогена под действием электронов π-связи. Атом галогена, приобретающий некоторый дробный положительный заряд, образует с электронами π-связи нестабильный интермедиат, называемый π-комплексом или комплексом с переносом заряда. Следует отметить, что в π-комплексе галоген не образует направленной связи с каким-нибудь конкретным атомом углерода; в этом комплексе просто реализуется донорно-акцепторное взаимодействие электронной пары π-связи как донора и галогена как акцептора.
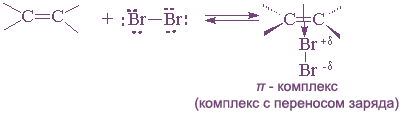
Далее π-комплекс превращается в циклический бромониевый ион. В процессе образования этого циклического катиона происходит гетеролитический разрыв связи Br-Br и пустая р-орбиталь sp2-гибридизованного атома углерода перекрывается с р-орбиталью "неподеленной пары" электронов атома галогена, образуя циклический ион бромония.
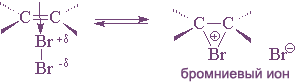
На последней, третьей стадии анион брома как нуклеофильный агент атакует один из атомов углерода бромониевого иона. Нуклеофильная атака бромид-иона приводит к раскрытию трехчленного цикла и образованию вицинального дибромида (vic-рядом). Эту стадию формально можно рассматривать как нуклеофильное замещение SN2 у атома углерода, где уходящей группой является Br+.

Результат этой реакции нетрудно предвидеть: анион брома атакует карбкатион с образованием дибромэтана.
Быстрое обесцвечивание раствора брома в СCl4 служит одним из простейших тестов на ненасыщенность, поскольку и алкены, и алкины, и диены быстро реагируют с бромом.
H2С = СН2 + НВr → Н3С - CH2Вr
Присоединение галогенводородов к гомологам этилена идет по правилу В.В.Марковникова (1837 - 1904):

Правило Марковникова можно объяснить тем, что у несимметричных алкенов (например, в пропилене) электронная плотность распределена неравномерно. Под влиянием метильной группы, связанной непосредственно с двойной связью, происходит смещение электронной плотности в сторону этой связи (на крайний углеродный атом).
Вследствие такого смещения p-связь поляризуется и на углеродных атомах возникают частичные заряды. Легко представить, что положительно заряженный ион водорода (протон) присоединится к атому углерода (электрофильное присоединение), имеющему частичный отрицательный заряд, а анион брома - к углероду с частичным положительным зарядом.
Такое присоединение является следствием взаимного влияния атомов в органической молекуле. Как известно, электроотрицательность атома углерода немного выше, чем водорода.
Поэтому в метильной группе наблюдается некоторая поляризация σ-связей С-Н, связанная со смещением электронной плотности от водородных атомов к углероду. В свою очередь это вызывает повышение электронной плотности в области двойной связи и особенно на ее крайнем, атоме. Таким образом, метильная группа, как и другие алкильные группы, выступает в качестве донора электронов. Однако в присутствии пероксидных соединений или О2 (когда реакция имеет радикальный характер) эта реакция может идти и против правила Марковникова.
По тем же причинам правило Марковникова соблюдается при присоединении к несимметричным алкенам не только галогеноводородов, но и других электрофильных реагентов (H2O, H2SО4, НОСl, ICl и др.).
H3C - CH = CH2 + H - OH → H3C - CHOH - CH3 (изопропиловый спирт)
Реакции окисления
Алкены окисляются легче, чем алканы. Продукты, образованные при окислении алкенов, и их строение зависят от строения алкенов и от условий проведения этой реакции.
Н2С = СН2 + 3O2 → 2СO2 + 2Н2O

3H2C = CH2 + 2KMnO4 + 4H2O → 3HOCH2 - CH2OH (этиленгликоль)+ 2MnO2 + KOH
Эта реакция является качественной: фиолетовая окраска раствора перманганата калия изменяется при добавлении к нему непредельного соединения.
В более жестких условиях (окисление КМnO4 в присутствии серной кислоты или хромовой смесью) в алкене происходит разрыв двойной связи с образованием кислородсодержащих продуктов:
H3C - CH = CH - CH3 + 2O2 → 2H3C - COOH (уксусная кислота)
Реакция изомеризации
При нагревании или в присутствии катализаторов алкены способны изомеризоваться - происходит перемещение двойной связи или установление изостроения.
Реакции полимеризации
За счет разрыва π-связей молекулы алкена могут соединяться друг с другом, образуя длинные цепные молекулы.
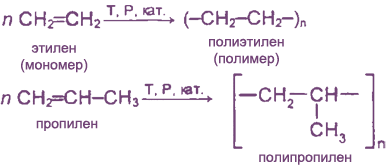
Нахождение в природе и физиологическая роль алкенов
В природе ациклические алкены практически не встречаются. Простейший представитель этого класса органических соединений - этилен C2H4 - является гормоном для растений и в незначительном количестве в них синтезируется.
Один из немногих природных алкенов - мускалур (цис-трикозен-9) является половым аттрактантом самки домашней мухи (Musca domestica).
Низшие алкены в высоких концентрациях обладают наркотическим эффектом. Высшие члены ряда также вызывают судороги и раздражение слизистых оболочек дыхательных путей
Отдельные представители
Этилен - вызывает наркоз, обладает раздражающим и мутагенным действием.
Этилен - самое производимое органическое соединение в мире; общее мировое производство этилена в 2008 году составило 113 миллионов тонн и продолжает расти на 2-3% в год.
Этилен является ведущим продуктом основного органического синтеза и применяется для получения полиэтилена (1-е место, до 60 % всего объёма).
Представляет собой воскообразную массу белого цвета (тонкие листы прозрачный бесцветны). Химически- и морозостоек, изолятор, не чувствителен к удару (амортизатор), при нагревании размягчается (80-120°С), при охлаждении застывает, адгезия (сцепление поверхностей разнородных твёрдых и/или жидких тел) - чрезвычайно низкая. Иногда в народном сознании отождествляется с целлофаном - похожим материалом растительного происхождения.
Пропилен - вызывает наркоз (сильнее, чем этилен), оказывает общетоксическое и мутагенное действие.
Устойчив к действию воды, не реагирует с щелочами любой концентрации, с растворами нейтральных, кислых и основных солей, органическими и неорганическими кислотами, даже концентрированной серной кислоты, но разлагается при действии 50%-ой азотной кислоты при комнатной температуре и под воздействием жидкого и газообразного хлора и фтора. Со временем, происходит термостарение.
- Полиэтиленовая плёнка (особенно упаковочных, например, пузырчатая упаковка или скотч ).


- Тара ( бутылки , банки , ящики , канистры , садовые лейки , горшки для рассады.
- Полимерные трубы для канализации , дренажа , водо-, газоснабжения.

- Электроизоляционный материал.
- Полиэтиленовый порошок используется как термоклей.