Строение атома и атомного ядра. Изотопы
Слово" атом" переводится с древнегреческого языка как "неделимый".
Атомы - мельчайшие частицы вещества.
Строение атома
В конце XIX - начале XX века физики доказали, что
атом является сложной частицей и состоит из более простых (элементарных) частиц. Были обнаружены:
· катодные лучи
(английский физик Дж. Дж. Томсон ,1897 г.),частицы которых получили название электроны e- (несут единичный отрицательный заряд);
· естественная радиоактивность
элементов (французские ученые - радиохимики А. Беккерель и М. Склодовская-Кюри, физик Пьер Кюри, 1896 г.) и существование α-частиц ( ядер
гелия 4He2+);
· наличие в центре атома положительно заряженного ядра (английский физик и радиохимик Э. Резерфорд , 1911 г.);
· искусственное превращение одного элемента в другой , например азота в кислород (Э. Резерфорд , 1919 г.). Из ядра атома одного элемента (азота - в опыте Резерфорда) при соударении с α-частицей образовывалось ядро атома другого элемента (кислорода) и новая частица, несущая единичный положительный заряд и названная протоном (p+, ядро 1H)
· наличие в ядре атома электронейтральных частиц - нейтронов n0 (английский физик Дж. Чедвик , 1932 г.). В результате проведенных исследований было установлено, что в атоме каждого элемента (кроме 1H) присутствуют протоны , нейтроны и электроны , причем протоны и нейтроны сосредоточены в ядре атома, а электроны - на его периферии (в электронной оболочке).
Электроны принято обозначать так : e−.
Электроны e−очень легкие, почти невесомые, но зато имеют отрицательный
электрический заряд. Он равен -1. Электрический ток, которым все мы пользуемся - это поток электронов, бегущий в проводах.
Нейтроны обозначают так : n0 , а протоны так : p+ .
По массе нейтроны и протоны почти одинаковы.
Число протонов в ядре равно числу электронов в оболочке атома и отвечает порядковому номеру этого элемента в Периодической системе.
Атомное ядро
- центральная часть
атома, в которой сосредоточена основная его масса и структура которого определяет химический элемент, к которому относится атом.
Атомное ядро состоит из нуклонов
- положительно заряженных
протонов p+ и нейтральных нейтронов n0 , которые связаны между собой при помощи сильного взаимодействия. Атомное ядро, рассматриваемое как класс частиц с определённым числом протонов и нейтронов, часто называется нуклидом.
Количество протонов в ядре называется его зарядовым числом Z
- это число равно порядковому номеру элемента, к которому относится атом в таблице Менделеева .
Число нейтронов в ядре обозначается буквой N , а число протонов
- буквой
Z. Эти числа связаны между собой простым соотношением:
A = Z + N
Полное количество нуклонов в ядре называется его массовым числом A = N + Z и приблизительно равно средней массе атома, указанной в таблице Менделеева.
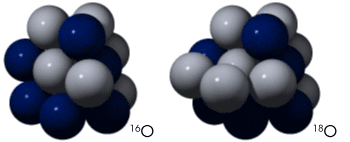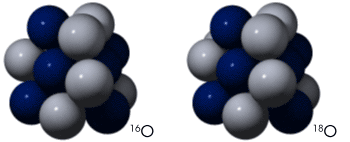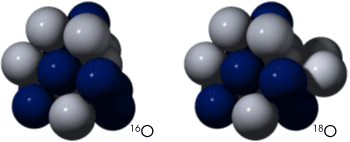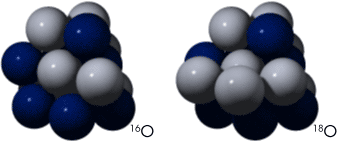
Ядра атомов с одинаковым числом протонов и разным числом нейтронов называются изотопами.
Многие элементы имеют по одному природному изотопу, например, Be, F, Nа, Al, P, Mn,Co, I, Au и некоторые другие. Но большинство элементов имеют по два, по три иболее устойчивых изотопа.
Например:
Ядра атомов с одинаковым числом нейтронов, но разным числом протонов - называются изотонами .
Атомы различных элементов с одинаковой атомной массой-А называются изобарами.